
VENTANA MMR RxDx Panel
tolkningsguide för endometriellt
karcinom (EC)
VENTANA anti-MLH1 (M1) Mouse Monoclonal Primary Antibody
VENTANA anti-PMS2 (A16-4) Mouse Monoclonal Primary Antibody
VENTANA anti-MSH2 (G219-1129) Mouse Monoclonal Primary Antibody
VENTANA anti-MSH6 (SP93) Rabbit Monoclonal Primary Antibody


Innehållsförteckning
Inledning 1
Avsedd användning 3
Produktens avsedda användning 3
Syftet med tolkningsguiden 3
Klinisk utvärdering 4
Färgningsegenskaper 4
Acceptanskriterier för morfologi och bakgrund 5
Fallkriterier för klinisk utvärdering 5
Tolkningssalgoritm 6
Kontroller 8
Interna positiva kontroller 8
Arbetsflöde för prov 10
Referensbilder 12
Kvalificerade fall 12
Ej kvalificerade fall 14
Utmanande fall 18
Inverkan av föranalytiska förhållanden på VENTANA MMR RxDx Panel 28
Godtagbara fixeringsvillkor för att uppnå optimala färgningsresultat 28
Stabilitet hos snitt i objektglas 32
Snittjocklek 32
Referenser 33


Reparation av felparat DNA (MMR) är en bevarad molekylär
mekanism som arbetar för att korrigera de felaktiga basparningar
som spontant inträffar vid DNA-replikering. Metoder som baseras
på en polymeraskedjereaktion (PCR) har visat att MMR-fel ofta
leder till mikrosatellitinstabilitet (MSI), ett tillstånd där korta
tandemupprepningar av nukleotider infogas i DNA:t. När antalet
upprepningar är lika med eller högre än 30% av undersökta
mikrosatellitloci kan MSI vidare karakteriseras som MSI-High
(MSI-H). Defekter i MMR-maskineriet har tillskrivits mutationer i
MMR-proteinerna, oftast MLH1, PMS2, MSH2 och MSH6.
MLH1- och PMS2-proteinerna fungerar normalt tillsammans
i ett heterodimert komplex, liksom MSH2- och MSH6-
proteinerna. När MMR fungerar normalt binds MSH6-/MSH2-
heterodimer till felparat DNA. Denna bindning framkallar en
konformationsändring som gör att MLH1-/PMS2-heterodimern
kan binda det DNA-bundna MSH6-/MSH2-komplexet, vilket
resulterar i excisionsreparation av det berörda DNA:t.
Mutationer eller brister i dessa proteiner leder till frekvent MSI
och somatisk mutation på grund av replikeringsfel. MMR-
immunhistokemi (IHC) kan visa sig vara användbart för att
identifiera MMR-gener som sannolikt innehåller germinala eller
somatiska förändringar.
Traditionellt har behandlingen för cancerpatienter dikterats av
den specifika cancerformen. Framväxande immunbehandlingar,
särskilt sådana som ändrar cellvägar som rör proteiner för
programmerad celldöd 1 (PD-1) eller liganden för programmerad
celldöd 1 (PD-L1) förändrar dock klinikers behandlingsstrategier.
PD-1 är en hämmande receptor som uttrycks på T-celler efter
T-cellsaktivering och som upprätthålls vid kronisk stimulering,
till exempel kronisk infektion eller cancer. PD-L1-uttryck har
observerats i immunceller och maligna celler, och ett avvikande
uttryck av PD-L1 på tumörceller (TC) har rapporterats hindra
anti-tumörimmunitet, vilket leder till immunavvikelse. Därför är
det lockande att avbryta PD-L1/PD-1-vägen för att återuppliva
tumörspecifik T-cellsimmunitet.
MMR-proteiner (MLH1, PMS2, MSH2 och MSH6) uttrycks allmänt
i spridningen av normala och maligna celler. Många vanliga
cancerformer har defekt MMR (dMMR) och uppvisar MSI. Flera
studier har visat att defekt MMR sammanfaller med ett högre
uttryck av PD-1- eller PD-L1-proteiner. Därmed kan MMR-
proteiner vara användbara som prediktiva biomarkörer för PD-1-
inriktad behandling. Specifikt kan avsaknad av uttryck för ett eller
flera MMR-proteiner förutsäga en ökad sannolikhet för att svara
på sådan behandling. PD-1-hämmare kan vara främjande vid
många vanliga cancertyper med hög frekvens av defekt MMR
och/eller MSI-H oavsett cancerns ursprungsvävnad. Därför
kommer patienter där PD-1-inriktad behandling övervägs att
gynnas av en behandlingsvägledande diagnostisk analys för att
identifiera patientpopulationen med defekt MMR.
Endometriellt karcinom (EC) är en av de vanligaste gynekologiska
maligniteterna.
12
Det konstateras ofta ha många genetiska
förändringar, inklusive MSI.
12
Det har också föreslagits att
MSI EC kan ha ökat uttryck av PD-L1-protein i jämförelse
med mikrosatellitstabil (MSS) EC.
16
Behandlingen av EC
beror på sjukdomens grad, histologi och stadium,
17
men en
utvärdering av EC-tumörernas MMR-status underlättar för att
ställa prognos och vägleda behandlingen
12
. Därför kommer
patienter där PD-1-inriktad behandling övervägs att gynnas av
en behandlingsvägledande diagnostisk analys för att identifiera
MMR-statusen.
Avsaknad av uttryck av något av de väsentliga MMR-proteinerna,
inklusive MLH1, PMS2, MSH2 eller MSH6, orsakar defekt MMR.
Förekomst av färgning för alla fyra MMR-proteinmarkörer i
tumören indikerar att fallet är kvalificerat för VENTANA MMR IHC-
status. Avsaknad av färgning i någon av MMR-proteinmarkörerna
för VENTANA MMR RxDx Panel anger att ett fall inte är kvalificerat
för VENTANA MMR IHC-status.
Inledning
VENTANA MMR RxDx Panel för endometriellt karcinom 1

2 VENTANA MMR RxDx Panel för endometriellt karcinom

Avsedd användning
Produktens avsedda användning
Läs aktuell bipacksedel till VENTANA MMR RxDx Panel för
en detaljerad beskrivning av avsedd användning för den här
produkten, inklusive associerade indikationer.
Syftet med tolkningsguiden
Den här guiden är till för att:
• Ge patologer ett verktyg för att underlätta den kliniska
utvärderingen av formalinfixerade, paraffininbäddade (FFPE)
tumörsnitt som färgats med VENTANA MMR RxDx Panel i
enlighet med föreslagen produktmärkning.
• Tillhandahålla fotografiska bilder som illustrerar de
färgningsmönster som kan uppstå vid färgning av tumörceller
med VENTANA MMR RxDx Panel.
• Ge exempel på bilder av utmanande fall för att ge vägledning
vid utvärdering av sådana.
• Ge vägledning vid användning av MMR-proteinpositiva
normala vävnadselement som fungerar som en positiv intern
kontroll när de färgas med VENTANA MMR RxDx Panel.
VENTANA MMR RxDx Panel för endometriellt karcinom 3

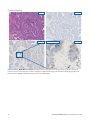
MMR intakt uttryck och förlust av färgningsuttryck: I dessa fall av endometriellt karcinom uppvisar kärnorna en entydig
färgning, vilket är det dominerande färgningsmönstret i de flesta tumörvävnader i MSH6 intakt uttryck (vänster bild). Frånvaro av
nukleär färgning i tumörvävnad representerar MSH6 förlust av uttryck (höger bild). Entydig nukleär färgning i interna kontrollceller
(d.v.s. lymfocyter) i närheten av livskraftiga tumörer fungerar som godtagbara interna positiva kontroller.
Färgningsegenskaper
Klinisk utvärdering
Celler som är märkta med varje analys i VENTANA MMR
RxDx Panel utvärderas för förekomst eller frånvaro av
diaminobenzidinesignalen (DAB). VENTANA MMR RxDx Panel-
färgning i MMR-proteiner följer ett nukleärt mönster. Frånvaro av
någon av MMR-proteinerna som detekteras av VENTANA MMR
RxDx Panel observeras i tumörcellernas kärnor. MMR-statusen
klassificeras som intakt uttryck eller förlust av uttryck, endast
baserad på entydig nukleär färgning.
• Intakt uttryck kännetecknas av tumörceller som uppvisar
entydig färgning som är lika med eller större än intensiteten
hos interna kontroller ovanför bakgrunden.
• Förlust av uttryck kännetecknas av att det inte finns någon
detekterbar signal. Fall med förlust av uttryck kan fortfarande
uppvisa en blekgrå missfärgning av cellkärnorna.
Signalen kan fördelas jämnt och ha en enhetlig intensitetsnivå i
hela tumörens neoplastiska delar eller fördelas heterogent med
mer än en intensitetsnivå. Den ska lätt kunna detekteras vid
lågeffektförstoringar som 2x eller 4x. En grafisk representation
av VENTANA MMR RxDx Panel-märkta neoplastiska celltyper/
färgningselement finns i avsnittet Referensbilder i den här
tolkningsguiden. Den artmatchade, negativa reagenskontrollen
(NRC) används för att utvärdera förekomst av bakgrund i
testprover och för att upprätta en baslinje för färgningsintensitet.
Acceptanskriterier för morfologi och bakgrund anges i tabell 1.
Fallkriterier för utvärdering av MMR-status hos neoplastisk vävnad
med någon av de fyra analyserna i VENTANA MMR RxDx Panel
finns i tabell 2.
Frånvaro av nukleär
färgning i tumörceller
Entydig nukleär
färgning i tumörceller
Stark nukleär färgning i
lymfocyter
4 VENTANA MMR RxDx Panel för endometriellt karcinom
MSH6 10x MSH6 10x

Acceptanskriterier för morfologi och bakgrund
För varje fall som färgas med VENTANA MMR RxDx Panel bedöms acceptansen för vävnadsmorfologi och bakgrund enligt kriterierna i
tabell 1.
Fallkriterier för klinisk utvärdering
Tabell 2 sammanfattar kriterierna för ett objektglas med neoplastisk vävnad som ska utvärderas för MMR-status med någon av
analyserna i VENTANA MMR RxDx Panel.
Kriterier Godtagbart Ej godtagbart
Morfologi Cellelement av intresse visualiseras, vilket
möjliggör klinisk tolkning av specifik färgning
Cellelement av intresse visualiseras inte, vilket
omöjliggör klinisk tolkning av specifik färgning
Bakgrund Bakgrunden påverkar inte den kliniska
tolkningen av specifik färgning
Bakgrunden stör möjligheten att tolka specifik
färgning
Tabell 1: Acceptanskriterier för morfologi och bakgrund
Klinisk tolkning Kriterier för färgningsmönster
Utvärderbar (alla måste vara sanna)
1. H&E har ≥ 50 livskraftiga tumörceller
2. Objektglaset med Negative Reagent Control är godtagbart
3. Morfologin är godtagbar
4. Bakgrunden är godtagbar
5. Interna positiva kontroller har en entydig nukleär färgning
Ej utvärderbar (om ett av kriterierna i
detta avsnitt är uppfyllt ska färgningen av
objektglaset upprepas eller fallet avvisas, i
förekommande fall)
1. H&E har < 50 livskraftiga tumörceller
2. Objektglaset med Negative Reagent Control är ej godtagbart
3. Morfologin är ej godtagbar
4. Bakgrunden är ej godtagbar
5. Interna positiva kontroller har inte en entydig nukleär färgning
6. Tolkning är inte möjlig på grund av vävnadsförlust, tumörfrånvaro,
artefakter och/eller kantartefakter
Tabell 2: Kriterier för utvärderbar och ej utvärderbar
VENTANA MMR RxDx Panel för endometriellt karcinom 5

VENTANA MMR RxDx Panel består av fyra analyser: VENTANA
anti-MLH1 (M1) Mouse Monoclonal Primary Antibody, VENTANA
anti-PMS2 (A16-4) Mouse Monoclonal Primary Antibody,
VENTANA anti-MSH2 (G219-1129) Mouse Monoclonal Primary
Antibody och VENTANA anti-MSH6 (SP93) Rabbit Monoclonal
Primary Antibody. Ett seriellt vävnadssnitt av testprovet behövs för
färgning med var och en av dessa antikroppar. Ytterligare seriella
vävnadssnitt av testprovet behövs för färgning med hematoxylin
och eosin (H&E) och med NRC-antikropp som motsvarar arten
av respektive VENTANA MMR RxDx Panel-antikropp (Negative
Control (Monoclonal) (mNRC) eller Rabbit Monoclonal Negative
Control Ig (rNRC)).
Neoplastiska celler som är färgade med VENTANA MMR
RxDx Panel utvärderas för förekomst eller frånvaro av DAB-
signalen. Det matchade, NRC-färgade objektglaset används
för att bedöma icke-specifik bakgrundsfärgning och graden
av bakgrundsfärgning som man vet förekommer på grund av
specifika vävnadselement (se kvalificerade och ej kvalificerade
fallbilder).
Om H&E-utvärderingen visar att patientprovet är otillräckligt (till
exempel om det finns färre än 50 livskraftiga tumörceller) bör ett
nytt prov tas.
Upprepad färgning av ett prov för en viss MMR RxDx-analys inom
panelen (t.ex. VENTANA anti-MLH1 (M1) Mouse Monoclonal
Primary Antibody) ska utföras på ofärgade objektglas om (1)
fallets objektglas färgat med lämplig NRC för den analysen
inte uppvisar godtagbar färgning, eller (2) om fallets objektglas
färgat med den specifika MMR RxDx-analysen (t.ex. VENTANA
anti-MLH1 (M1) Mouse Monoclonal Primary Antibody) inte
är utvärderbart. Om något av objektglasen inte kan tolkas på
grund av bristande färgning i de interna positiva kontrollcellerna,
förekomst av artefakter, kanteffekter, nekros, brist på vävnad eller
av någon annan orsak, går det inte att utvärdera objektglaset. Om
kontrollfärgningen är godtagbar och de VENTANA MMR RxDx
Panel-färgade objektglasen kan utvärderas, kan detta göras av en
utbildad patolog enligt beskrivningen i tolkningsalgoritmen.
OBS! OptiView DAB IHC Detection Kit och OptiView Amplification
Kit är de enda detektionsreagenserna som rekommenderas för
användning med VENTANA MMR RxDx Panel.
Tolkningarna för proteinuttryck och MMR-status för VENTANA
MMR RxDx Panel anges nedan i tabellerna 3 och 4. Representativa
fall diskuteras i avsnittet Referensbilder.
Utvärdera VENTANA MMR RxDx Panel:
Tolkningssalgoritm
Tabell 4: Tolkning av MMR-status med VENTANA MMR RxDx Panel
Kvalificerad Ej kvalificerad
Alla fyra proteiner (MLH1, PMS2, MSH2 och MSH6) i
panelen uppvisar ett intakt uttryck
Minst ett protein (MLH1, PMS2, MSH2 eller MSH6) i panelen
uppvisar förlust av uttryck
Tabell 3: Tolkning av proteinuttryck med VENTANA MMR RxDx Panel
Intakt proteinuttryck Förlust av proteinuttryck
Entydig nukleär färgning i livskraftiga tumörceller vid
förekomst av godtagbara interna positiva kontroller
(t.ex. nukleär färgning i lymfocyter, fibroblaster eller
normalt epitel i närheten av tumören)
Entydig förlust av nukleär färgning eller fokal, svag, tvetydig
nukleär färgning i livskraftiga tumörceller vid förekomst av
godtagbara interna positiva kontroller. Punktvis nukleär färgning
anses som negativ
6 VENTANA MMR RxDx Panel för endometriellt karcinom

Endometriellt karcinom – Kvalificerad för klinisk diagnos
MSH2 intakt uttryck: Stark nukleär
färgning vid förekomst av godtagbara
interna positiva kontroller
PMS2 intakt uttryck: Stark nukleär
färgning vid förekomst av godtagbara
interna positiva kontroller
MLH1 intakt uttryck: Stark nukleär
färgning vid förekomst av godtagbara
interna positiva kontroller
Endometriellt karcinom – Ej kvalificerad för klinisk diagnos
MLH1 förlust av uttryck: Frånvaro
av nukleär färgning vid förekomst av
godtagbara interna positiva kontroller
MSH6 förlust av uttryck: Frånvaro
av nukleär färgning vid förekomst av
godtagbara interna positiva kontroller
MSH2 förlust av uttryck: Frånvaro
av nukleär färgning vid förekomst av
godtagbara interna positiva kontroller
MLH1 20x MSH6 20x MSH2 20x
MSH2 20x
PMS2 20x
MLH1 20x
MSH2-
positiva
kärnor
PMS2-
positiva
kärnor
MLH1-
positiva
kärnor
VENTANA MMR RxDx Panel för endometriellt karcinom 7

Kontroller
Vid färgning med VENTANA MMR RxDx Panel visar normala
vävnadselement, såsom lymfocyter, fibroblaster eller normalt
epitel, i närheten av tumören nukleär färgning av MMR-proteiner.
Dessa vävnadselement fungerar som interna positiva kontroller
och måste vara godtagbara för att det färgade objektglaset
för varje analys i panelen ska kunna utvärderas. Interna
kontroller måste utvärderas för varje analys och måste uppfylla
färgningskriterierna för en paneltolkning av MMR-status. I
avsaknad av entydig nukleär färgning i lymfocyter, fibroblaster
eller normalt epitel i närheten av tumören ska det färgade
objektglaset i analysen anses vara ”ej utvärderbart”.
Tabell 5 beskriver kriterierna för godtagbar intern
kontrollfärgning.
Utvärderbar Ej utvärderbar
Förekomst av entydig nukleär färgning i normala
vävnadselement (t.ex. lymfocyter, fibroblaster eller normalt
epitel) i närheten av tumören
Frånvaro av entydig nukleär färgning i normala vävnadselement
(t.ex. lymfocyter, fibroblaster eller normalt epitel) i närheten av
tumören
Tabell 5: Kriterier för intern kontrollfärgning
Intern positiv kontroll, fall 1: Endometriellt karcinom uppvisar ingen intern kontrollfärgning i närheten av tumörcellerna och kan
därför inte utvärderas. Den godtagbara Negative Reagent Control som visas är mus NRC (mNRC).
Interna positiva kontroller
Representativa bilder av den interna kontrollen för VENTANA MMR RxDx Panel visas nedan.
8 VENTANA MMR RxDx Panel för endometriellt karcinom
H&E 40x mNRC 40x MLH1 40x

Intern positiv kontroll, fall 2: Stark intern färgning av kontrollcell uppvisas i närheten av tumören i ett fall av endometriellt karcinom
med MLH1 förlust av uttryck och ett fall med MSH2 intakt uttryck. Godtagbar Negative Reagent Control är mus NRC (mNRC).
MLH1 20x
Färgning av intern kontrollcell Färgning av intern kontrollcell
VENTANA MMR RxDx Panel för endometriellt karcinom 9
H&E 20x mNRC 20x
MSH2 20x

Arbetsflöde för prov
Testning med VENTANA MMR RxDx Panel kräver flera seriella
vävnadssnitt av varje testprov. Ett snitt var behövs för färgning
med var och en av de 4 analyserna: VENTANA anti-MLH1 (M1)
Mouse Monoclonal Primary Antibody, VENTANA anti-PMS2 (A16-
4) Mouse Monoclonal Primary Antibody, VENTANA anti-MSH2
(G219-1129) Mouse Monoclonal Primary Antibody och VENTANA
anti-MSH6 (SP93) Rabbit Monoclonal Primary Antibody.
Dessutom behövs snitt från varje testprov till färgning med H&E
och med NRC-antikropp som motsvarar respektive VENTANA
MMR RxDx Panel-antikropp (mNRC eller rNRC).
Om H&E-utvärderingen visar att patientprovet är otillräckligt (till
exempel om det finns färre än 50 livskraftiga tumörceller) bör
ett nytt prov tas. Upprepad färgning av ett prov för en viss MMR
RxDx-analys inom panelen (t.ex. VENTANA anti-MLH1 (M1)
Mouse Monoclonal Primary Antibody) ska utföras på ofärgade
objektglas om (1) fallets objektglas färgat med lämplig negativ
reagenskontroll inte uppvisar godtagbar färgning, eller (2) om
fallets objektglas färgat med den specifika MMR RxDx-analysen
(t.ex. VENTANA anti-MLH1 (M1) Mouse Monoclonal Primary
Antibody) inte är utvärderbart. Om något av objektglasen inte
kan tolkas på grund av frånvaro av färgning i de interna positiva
kontrollcellerna, artefakter, kanteffekter, nekros, brist på vävnad
eller någon annan orsak, går det inte att utvärdera objektglaset.
Om kontrollerna är godtagbara och de VENTANA MMR RxDx
Panel-färgade objektglasen kan utvärderas, kan detta göras av en
utbildad patolog enligt beskrivningen i tolkningsalgoritmen.
OBS! OptiView DAB IHC Detection Kit och OptiView Amplification
Kit är de enda detektionsreagenserna som rekommenderas för
användning med VENTANA MMR RxDx Panel.
10 VENTANA MMR RxDx Panel för endometriellt karcinom

Provflöde
VENTANA MMR RxDx Panel för endometriellt karcinom 11
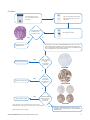
4 m tjocka snitt monteras på positivt
laddade objektglas. (6 eller 7 seriella
snitt behövs)
Upprepa färgningen med
ett nytt patientprov*
Nej Ja
Är H&E-objektglaset
godtagbart (≥ 50
livskraftiga celler)?
Ett snitt färgas vid varje analys i VENTANA MMR RxDx Panel. Dessutom färgas
varje analystillstånd med artmatchad negativ reagenskontroll, Negative Control
(Monoclonal) (mNRC), eller Rabbit Monoclonal Negative Control Ig (rNRC) enligt
vad som är tillämpligt vid samma instrumentkörning.
MMR (MLH1, PMS2, MSH2, MSH6)-resultatet fastställs av
en utbildad patolog enligt tolkningsalgoritmen till VENTANA
MMR RxDx Panel.
Nej
Nej
Nej
Ja
Ja
Ja
Är den negativa
reagenskontrollens
färgade
provobjektglas
godtagbart?
Uppvisar
varje färgat
provobjektglas
godtagbara interna
kontroller?
Är VENTANA MMR
RxDx Panel-färgade
provobjektglas
godtagbara?
Tumör H&E
Tumör NRC
* Upprepning kan ske på samma patientblock eller ett annat
vävnadsblock från samma patient, beroende på vad som är tillämpligt.
(Alla tumörbilder vid 20x förstoring)
Intern kontroll
Tumör IHC
Tumörvävnadsprovet fixeras i
10% neutral buffrad formalin i
6–72 timmar.
Ett snitt färgas med H&E.
Upprepa färgningskörningen
Upprepa färgning av fallet*
Upprepa färgning av fallet*

12 VENTANA MMR RxDx Panel för endometriellt karcinom
Referensbilder
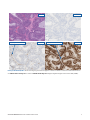
Kvalificerat fall 1: MLH1, PMS2, MSH2 och MSH6 intakt uttryck vid endometriellt karcinom som uppvisar stark nukleär färgning
i tumörceller vid förekomst av lämpligt färgade interna kontroller. De godtagbara Negative Reagent Controls som anges är mus NRC
(mNRC) och kanin NRC (rNRC).
Kvalificerade fall
mNRC 20x
rNRC 20x
MLH1 20x PMS2 20x
MSH2 20x MSH6 20x
H&E 20x

VENTANA MMR RxDx Panel för endometriellt karcinom 13
Kvalificerat fall 2: MLH1, PMS2, MSH2 och MSH6 intakt uttryck vid endometriellt karcinom som uppvisar stark nukleär färgning i
tumörceller vid förekomst av lämpligt färgade interna kontroller. Godtagbara Negative Reagent Controls är mus NRC (mNRC) och kanin
NRC (rNRC).
H&E 20x
mNRC 20x rNRC 20x
MLH1 20x PMS2 20x
MSH2 20x MSH6 20x

14 VENTANA MMR RxDx Panel för endometriellt karcinom
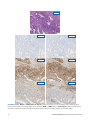
Ej kvalificerat fall 1: MLH1 och PMS2 förlust av uttryck vid endometriellt karcinom som inte uppvisar någon nukleär färgning i
tumörceller vid förekomst av lämpligt färgade interna kontroller. MSH2 och MSH6 uppvisar intakt uttryck. Cytoplasmisk färgning ska
inte beaktas vid tolkning av status. Godtagbara Negative Reagent Controls är mus NRC (mNRC) och kanin NRC (rNRC).
Ej kvalificerade fall
H&E 20x
mNRC 20x rNRC 20x
MLH1 20x PMS2 20x
MSH2 20x MSH6 20x

VENTANA MMR RxDx Panel för endometriellt karcinom 15
Ej kvalificerat fall 2: MLH1 och PMS2 förlust av uttryck vid endometriellt karcinom som inte uppvisar någon nukleär färgning i
tumörceller vid förekomst av lämpligt färgade interna kontroller. MSH2 och MSH6 uppvisar intakt uttryck. Cytoplasmisk färgning ska
inte beaktas vid tolkning av status. Godtagbara Negative Reagent Controls är mus NRC (mNRC) och kanin NRC (rNRC).
H&E 20x
mNRC 20x rNRC 20x
MLH1 20x PMS2 20x
MSH2 20x MSH6 20x

16 VENTANA MMR RxDx Panel för endometriellt karcinom
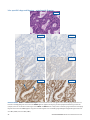
Ej kvalificerat fall 3: MSH2 och MSH6 förlust av uttryck vid endometriellt karcinom som inte uppvisar någon nukleär färgning i
tumörceller vid förekomst av lämpligt färgade interna kontroller. MLH1 och PMS2 uppvisar intakt uttryck. Cytoplasmisk färgning ska
inte beaktas vid tolkning av status. Godtagbara Negative Reagent Controls är mus NRC (mNRC) och kanin NRC (rNRC).
H&E 20x
mNRC 20x rNRC 20x
MLH1 20x PMS2 20x
MSH2 20x MSH6 20x
Sidan laddas...
Sidan laddas...
Sidan laddas...
Sidan laddas...
Sidan laddas...
Sidan laddas...
Sidan laddas...
Sidan laddas...
Sidan laddas...
Sidan laddas...
Sidan laddas...
Sidan laddas...
Sidan laddas...
Sidan laddas...
Sidan laddas...
Sidan laddas...
Sidan laddas...
Sidan laddas...
-
 1
1
-
 2
2
-
 3
3
-
 4
4
-
 5
5
-
 6
6
-
 7
7
-
 8
8
-
 9
9
-
 10
10
-
 11
11
-
 12
12
-
 13
13
-
 14
14
-
 15
15
-
 16
16
-
 17
17
-
 18
18
-
 19
19
-
 20
20
-
 21
21
-
 22
22
-
 23
23
-
 24
24
-
 25
25
-
 26
26
-
 27
27
-
 28
28
-
 29
29
-
 30
30
-
 31
31
-
 32
32
-
 33
33
-
 34
34
-
 35
35
-
 36
36
-
 37
37
-
 38
38
Roche BenchMark ULTRA Interpretation Guide
- Typ
- Interpretation Guide
- Denna manual är också lämplig för
Relaterade papper
-
Roche uPath PD-L1 image analysis for NSCLC IVD Algorithm Användarmanual
-
Roche NAVIFY Mutation Profiler Användarmanual
-
Roche BenchMark GX Användarmanual
-
Roche Virtuoso Användarmanual
-
Roche Virtuoso Användarmanual
-
Roche BenchMark ULTRA Användarmanual
-
Roche VENTANA HE 600 Användarmanual
-
Roche uPath IVD Användarmanual






































